导读:
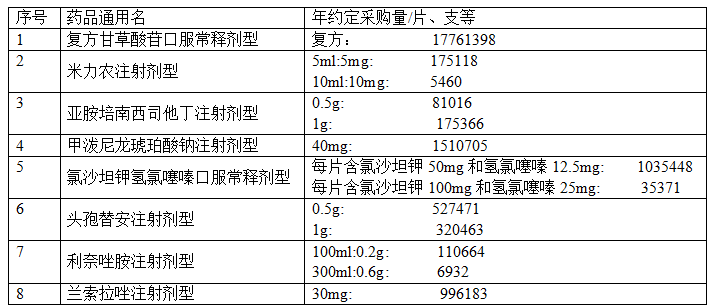
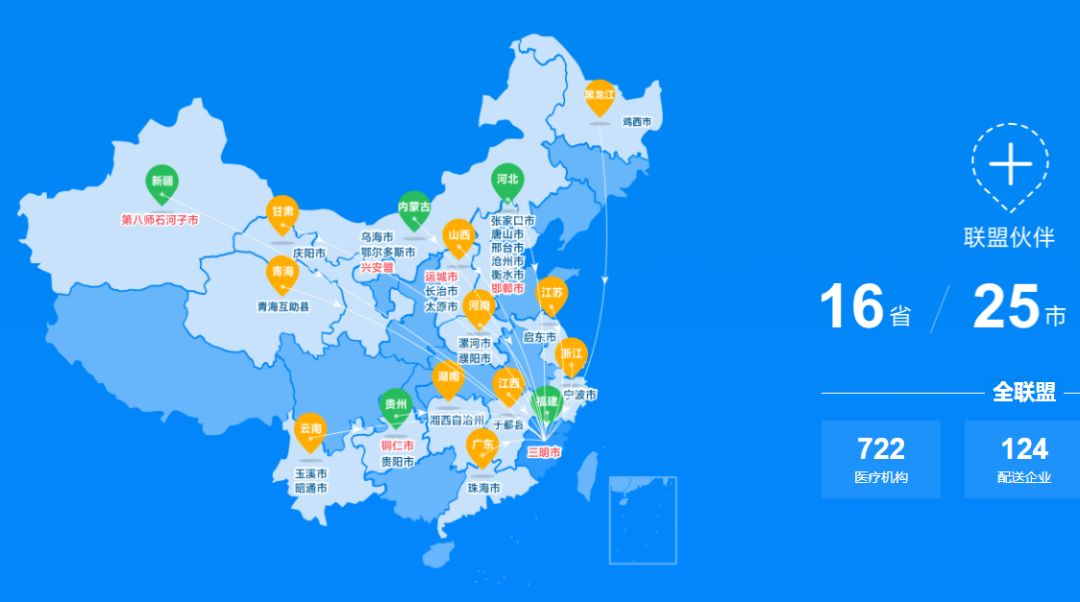
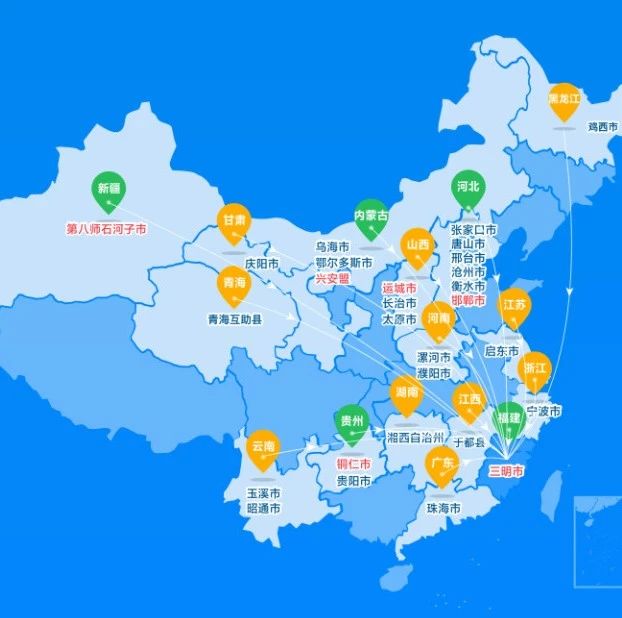
三明联盟试点开展非一致性评价药品的集中带量采购,通过以量换价挤压药品耗材虚高价格。三明联盟涵盖了16个省,25个城市。涉及到的8个品种,包括:复方甘草酸苷口服常释剂型、米力农注射剂型、亚胺培南西司他丁注射剂型、甲泼尼龙琥珀酸钠注射剂型、氯沙坦钾氢氯噻嗪口服常释剂型、头孢替安注射剂型、利奈唑胺注射剂型、兰索拉唑注射剂型。
为持续深化医药卫生体制改革,推进药品耗材联合限价采购,减轻群众用药负担。按照国家医疗保障局推进构建区域性采购联盟的工作部署,三明联盟试点开展非一致性评价药品的集中带量采购,通过以量换价挤压药品耗材虚高价格。现参照国家组织药品集中采购经验做法,制定本方案。
坚持“联合采购、量价挂钩、去除灰色、价格真实”的基本原则,参考省内各片区、联盟城市的药品采购价格作为限价,对未纳入国家组织集中采购和使用的药品开展带量采购。通过实行跨区域联盟带量采购,进一步提升联盟合作水平,实现保障临床用药需求、降低药品价格、减轻患者用药负担的目标,切实增强人民群众的就医获得感。
由参与试点采购的三明联盟城市委派代表组成联合采购办公室作为工作机构,共同负责本方案的实施,采购办公地点设三明市医疗保障局。
本次采购工作的开展依托“三明联盟”药械联合限价采购平台进行,所有公告和信息通过该平台公布,平台网址:http://sm.udplat.org/。
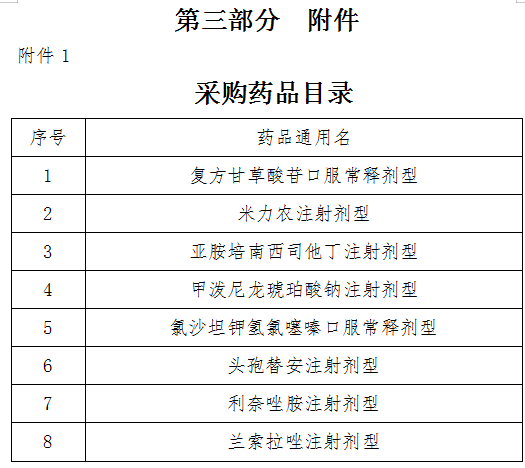
8种通用名下未通过一致性评价的药品。(详见附件1)
由各联盟地区根据需求确定实际采购数量(详见附件2)。入选企业全年产销能力需达到本次采购数量要求,各联盟地区保证完成约定采购量,若在采购周期内提前完成约定采购量的,超过部分仍按中选价供应使用,直至采购周期届满。
以完成约定采购量为原则,在集中采购结果执行日起一年作为一个采购周期。
在规定的时间内,参与竞选企业申报企业和产品资质。申报应由企业指定本企业正式员工完成,不得委托(挂靠经营的自然人)进行。企业申报的品种应包含采购品种目录内本企业生产的所有符合申报条件的规格,且必须包含至少一个采购品种目录指定的主品规。申报材料详见申报企业须知。
在与申报企业充分谈判的基础上,进行一轮竞价。企业报价即企业的实际供应价,应包含税费、配送费等在内的所有费用,以最小采购单元(即最小零售包装,如盒)进行报价,药品报价货币统一为人民币,单位为元。企业报价需严格遵循低价原则,申报的价格原则上不得高于本企业同品种在全国各省(市、区)的最低采购价格。
同一通用名的药品采取价低入选的办法进行评审。在保证质量的前提下,最低价者为拟入选药品,次低价者为备选。(同组别不同规格遵循差比价规则进行换算,剂型、包装、包材不做差比价计算,包装、包材须符合国家规定的标准,为临床常用包装。在价格相同情况下,添加附件的品规优先入选;如仍出现价格相同的情况,以2019年联盟地区同品种采购量大的企业优先入选。)
入选品规在“健康三明网”及“三明联盟”药械联合限价采购平台进行公布。
中选药品的配送由各联盟地区医保局根据各地实际情况牵头组织配送企业实施。参与本次采购的地区要统一回款方式,从药品验收入库并于采购平台确认之日算起,平均回款时间不超过30天。
(一)2020年3月27日8:00—4月2日17:00:企业注册,材料申报。
(三)2020年4月7日8:00—17:00:产品报名。
(五)2020年4月10—14日:与企业政策对接沟通。(期间将召开企业座谈会,具体时间地点另行通知)
(六)2020年4月15日9:00—15:00:企业模拟报价。
(七)2020年4月17日9:00—15:30:企业正式报价。
(九)2020年4月18日—21日:中选结果公示。
(十)2020年5月:各联盟城市签订带量购销合同,落实保障措施,采购备货。
根据疫情防控情况,以上时间如有变动,另行通知,请各企业及时关注采购平台发布信息。
(一)确保合法合规。参与集中采购的药品生产企业必须合法合规,在本次集中采购活动前两年内在医药购销领域无商业贿赂等不良记录、在药品生产活动中无严重违法违规记录、在GMP认证中无不予通过的情况。
(二)保障药品供应。严格执行“两票制”,且票货同行。中选企业是保障药品质量和供应的第一责任人,应积极配合联采办对其产品质量及供应情况进行的调查,按要求提供由药品监督管理部门设置或者确定的药品检验机构出具的药品检验报告书(每季度提供一批次),并及时、足量向配送企业发送药品。如出现不按合同供货、不能保障质量和供应等情况,将按照相关规定严肃处理。
(三)落实采购数量。中选结果公布后,各联盟城市及时组织签订带量购销合同,明确各方权利与责任,确保完成合同用量。
(四)严格违规处理。申报企业、中选企业、配送企业如发生违规行为(详见附件3),情节严重的将被列入“违规名单”。申报企业列入“违规名单”的,取消该企业的申报资格;中选企业列入“违规名单”的,取消中选资格,同时取消上述企业在列入“违规名单”之日起1年内参与联盟城市药品采购活动的资格;配送企业列入“违规名单”的,取消该企业的配送资格及列入“违规名单”之日起1年内参与联盟城市药品集中采购的配送资格。
(一)中选品种在各试点地区执行期间,若中选企业被列入“违规名单”,则立即停止中选品种的采购资格。备选品种经联采办确认后,各联盟城市及时组织采购。
(二)入选药品在履行承诺函中如有全国其他地区采购价格低于此次采购价格的,价格相应联动。
(三)中选药品在履行合同中如遇国家及各地药品采购政策调整,则结合实际制定对接政策。
本工作方案的解释权归三明联盟采购工作办公室,未尽事宜,另行通知。
实行企业自主申报及确认,在采购平台办理CA数字证书后,提交相关资质证明材料(电子版,所有证明材料全部加盖企业公章)。具体操作流程如下:
申报企业通过平台网站,线上填写企业资料提交申请;为保证信息准确,提交申请时平台会有二次确认要求,核对无误后确认提交。
本次采购只接受药品生产企业的申报。接受以集团公司名义进行申报,需递交集团从属关系证明材料。
药品供应企业只能授权一个自然人为管理员,负责本次药品联合限价采购活动的管理,并承担相应法律责任。集团公司所属全资及控股子公司可根据不同法人营业执照共同委托一个自然人作为授权代表。其他的自然人只能代表一个药品供应企业参加本次药品联合限价采购活动。
1.《企业营业执照》(正、副本复印件)。若为“三证合一”的新证书,无需填写第2、3项;
2.《组织机构代码证》(统一社会信用代码)(正、副本复印件);
4.《药品生产许可证》和《GMP证书》(正、副本复印件);
6.药品生产企业对经办人的《法定代表人授权书》(原件)和经办人身份证(正、反面复印件),以及为经办人办理社会保险的相关证明(复印件);
7.承诺函,内容包括无违法违规行为以及对产品的质量、售后服务、配送、货源保障的承诺(原件);
8、申报产品的《药品批准文号批件》(《注册批件》或者《再注册批件》,若有《药品注册补充批件》,请同时上传,以确保产品资质与实际情况相符)。
企业资质、产品资质审核通过后,企业才能从采购平台的药械库中勾选合规产品,进而完成产品报名。
在规定的截止时间前,药品供应企业可以修改或撤回申报材料。规定时间截止后,不得对其申报材料做任何修改,也不得撤销。
(一)药品供应企业在规定时间内通过采购平台对其产品进行报价,不报价或报价为0的产品视为自动放弃。
(三)企业报价即企业的实际供应价,应包含税费、配送费等在内的所有费用;申报企业须按药品产品的最小采购单位(即最小零售包装)进行报价,同企业不同规格报价须符合差比价规则,报价小数位数为2位,货币统一为人民币,单位为元。
(四)申报价不应高于本企业同品种全国各省(市、区)最低价。
(五)药品供应企业在报价时间截止后,不得修改报价,在报价周期时间内,用户可对单个产品进行多次报价操作,入选测算时每个产品的报价以最后一次报价价格为准。
申报企业、中选企业、配送企业如有以下行为,情节严重的将被列入“违规名单”。
(一)提供处方回扣或其他商业贿赂,进行非法促销活动;
(三)相互串通申报,排斥其他申报企业的公平竞争,损害采购方或者其他申报企业的合法利益;
(五)提供虚假证明文件及文献资料,或者以其他方式弄虚作假,骗取中选;
(八)中选企业、配送企业未按采购方以及法律法规要求实行配送;
(十二)中选药品中选后在规定的抽检或飞行检查中发现严重违背在申报材料中作出的承诺;
一、 复方甘草酸苷口服常释剂型年约定采购量(单位:片)
三、亚胺培南西司他丁注射剂型年约定采购量(单位:支)
四、甲泼尼龙琥珀酸钠注射剂型年约定采购量(单位:支)
五、氯沙坦钾氢氯噻嗪口服常释剂型年约定采购量(单位:片)
1、以上为采购平台收集数据,作采购基数,经各联盟城市审核确定后,以谈判竞价时公布数据为准,如有其他反馈意见请及时与联采办公室沟通。
2、方案公布后要跟进参与的联盟城市,请及时与联采办联系。
在审阅所有集中采购文件后,我方决定按照采购文件的规定参与申报。我方保证所提供的全部报价和其他证明文件的真实性、合法性。
我方已充分考虑到原材料价格等因素,并以此申报价格。如果我方药品中选,我方将按照采购方的要求供应中选药品,确保中选药品的价格、质量和数量等一切要素按照购销合同履行。
我方承诺,我方同联合采购办公室没有利益关系,不会为达成此项目同采购方进行任何不正当联系,不会在申报过程中有任何违法违规行为。