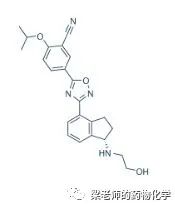
百时美施贵宝公司(Bristol-Myers Squibb)近天宣布,美国食品和药物管理局(FDA)批准0.92毫克的Zeposia(ozanimod)用于治疗复发性多发性成人硬化症(RMS),包括临床孤立的综合症,复发性疾病和活动性继发性进行性疾病。Zeposia,一种每日口服的口服药物,是唯一批准使用的鞘氨醇1-磷酸(S1P)受体调节剂,可为RMS患者提供无需进行基因检测即可开始使用。
多发性硬化症(MS)是一种免疫系统攻击覆盖神经的保护性髓鞘的疾病,造成破坏性损害,使信号很难在每个神经细胞之间传播。这种“信号故障”可能导致疾病和疾病复发。
Bristol Myers首席医学官Samit Hirawat医师表示:“ZEPOSIA在获得FDA批准后,患有复发性多发性硬化症的合适患者将可以选择另一种具有有意义疗效的口服治疗方案,以帮助解决该疾病的特征性复发和脑损伤。
SUNBEAM是基于一项关键的,三阶段,多中心,随机,双盲,双虚拟,主动对照试验,评估口服Zeposia(0.92 mg,相当于1 mg)相对每周肌肉内AVONEX®(干扰素)的疗效,安全性和耐受性beta-1a)治疗至少12个月。该研究包括20个国家中152个临床研究点的1,346人患有RMS的患者。
关于Zeposia(ozanimod)
Zeposia®是一种鞘氨醇1-磷酸(S1P)受体调节剂,与S1P受体1和5位具有高亲和力。Zeposia阻止淋巴细胞从淋巴结流出的能力,从而减少外周血中淋巴细胞的数量。Zeposia在多发性硬化症中发挥治疗作用尚不清楚,但可能涉及减少淋巴细胞向中枢神经系统的迁移。
Zeposia也正在开发其他免疫炎症指征,包括溃疡性结肠炎和克罗恩氏病。


药融圈致力于打造医药行业生态圈,共建、共创、共赢、共享,旨在解决生物医药发展过程中的共性关键问题(项目、资本、人才等),将平台的协同、联动、共享、共赢优势最大化实现并发挥,惠及千万企业。对大企业实现加速赋能,对中小企业实现助力孵化,形成企业服务领域新生态。药融圈围绕我国生物医药产业链,针对生物医药大数据、技术和资本投资、药融园(产业园)等开展系列系统性工作,促进我国生物医药产业健康发展,完善产业链,共同面对全球合作和竞争。